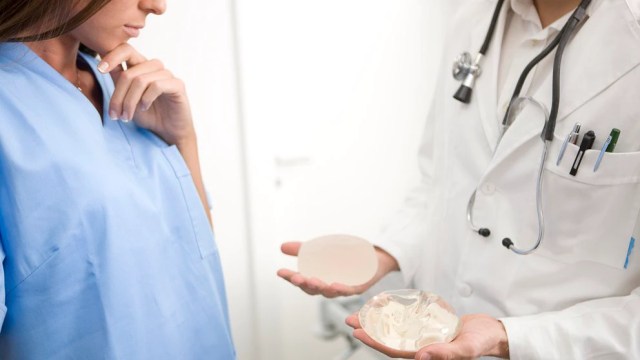
Son muchas las mujeres que luego de recibir un implante mamario tienen con el correr de los años alguna complicación. Entre las consecuencias, se encuentran la fatiga, erupción cutánea, pérdida de memoria y confusión mental, entre otros problemas de salud conocidos colectivamente como “enfermedad de los implantes mamarios”. Algunos implantes incluso, también se han relacionado con una forma de cáncer poco común y potencialmente mortal. Durante años, los activistas han buscado un proceso de consentimiento informado para que los pacientes tengan una comprensión clara de los riesgos y beneficios antes de optar por la cirugía.
Por Infobae
La nueva orden de la La Administración de Alimentos y Medicamentos (FDA) restringe la venta y distribución de implantes mamarios a proveedores e instalaciones que brindan a los pacientes una lista de verificación de riesgos, según publica el organismo. La lista de verificación “debe ser revisada con el posible paciente por el proveedor de atención médica para ayudar a garantizar que el paciente comprenda los riesgos, beneficios y otra información sobre el dispositivo de implante mamario”, dijo la agencia en un comunicado. Además, expresó que el paciente debe tener la oportunidad de firmar la lista de verificación de decisiones del paciente, que debe ser firmada por el médico que implanta el dispositivo.
Los reguladores también exigieron nuevas etiquetas de advertencia que acompañen a varios tipos de implantes mamarios. Esas etiquetas deben acompañar a la lista de verificación de decisiones del paciente e informar a las mujeres que reciben implantes rellenos de gel de silicona que deben someterse a exámenes periódicos para detectar posibles fugas por roturas. Las empresas tienen 30 días para publicar etiquetas actualizadas en sus sitios web.
“Al fortalecer los requisitos de seguridad para los fabricantes, la FDA está trabajando para cerrar las brechas de información para cualquier persona que pueda estar considerando la cirugía de implantes mamarios”, expresó Binita Ashar, directora de la Oficina de Dispositivos Quirúrgicos y de Control de Infecciones en el Centro de Dispositivos y Salud Radiológica.
El año pasado, los reguladores recomendaron que los fabricantes utilicen la precaución más estricta de la DFA, una advertencia incluida en un recuadro negro en la etiqueta del producto, para enumerar claramente las posibles complicaciones asociadas con los dispositivos. Esa guía también recomendó que los médicos usaran una lista de verificación de decisiones del paciente para guiar a los consumidores a través de los peligros potenciales.
El anuncio de este miércoles convirtió esas recomendaciones en un requisito para vender y distribuir implantes mamarios.
La lista de verificación del paciente enumera los riesgos comunes asociados con la cirugía de implantes mamarios, como dolor, cicatrices, asimetría e infección. También advierte sobre riesgos poco frecuentes que incluyen un cáncer del sistema inmunológico llamado linfoma anaplásico de células grandes asociado a implantes mamarios. La mayoría de los casos documentados del cáncer poco común y más de un tercio de las muertes relacionadas se relacionaron con implantes mamarios texturizados producidos por Allergan, que desde entonces han sido retirados del mercado.
La lista también advierte que “un implante mamario no es un dispositivo de por vida” y que eventualmente puede requerir remoción o reemplazo. Según la FDA , a una de cada 5 mujeres a las que se les colocan implantes se los extraen en un plazo de ocho a diez años. Tanto los implantes rellenos de gel de silicona como los de solución salina también pueden tener fugas o romperse. Debido a que las fugas son más difíciles de detectar en los implantes rellenos de gel de silicona, las mujeres que reciben ese tipo de dispositivo deben obtener imágenes periódicas para verificar si hay fugas, de acuerdo con la lista de verificación.
En 2019, varias mujeres que expresaron que sus implantes mamarios las dejaban con serios problemas de salud. Le dijeron a la FDA que el hecho de que los médicos no discutieran los riesgos las dejaba vulnerables. Describieron haber abandonado carreras y haber perdido tiempo con la familia debido a esos problemas.
El linfoma ligado a implantes mamarios es poco común. Los médicos en los Estados Unidos realizan alrededor de 400,000 cirugías con los implantes cada año y, a principios de 2020, la FDA había documentado 573 casos de cáncer en todo el mundo y 33 pacientes habían muerto a causa de él.
Aproximadamente las tres cuartas partes de los pacientes que reciben implantes toman la decisión por razones estéticas; el resto los recibe como parte de la reconstrucción después de la cirugía de cáncer de mama.
En 2010 un escándalo relacionado con prótesis mamarias ocupó parte de la agenda. La compañía francesa PIP, se supo, utilizaba un gel de silicona no homologado para uso médico, en vez del gel Nusil autorizado que declaraba emplear.
Se estima que medio millo?n de pro?tesis fraudulentas PIP fueron fabricadas y vendidas en el mundo entre 2001 y 2010, valiéndose de los ineficaces controles por parte de la empresa certificadora TU?V Rheinland